Après un workshop d’ouverture avec un focus sur les travaux et résultats du PFMG en oncogénomique, un grand nombre d’intervenants ont présenté leurs résultats s’appuyant sur des données produites grâce au PFMG.
Retrouvez ici la liste des abstracts recensés à cette occasion pour des posters ou des communications orales.
(si nous n’avons pas recensé votre abstract et que vous souhaitez qu’il soit ajouté à cette liste, n’hésitez pas à envoyer un mail à contact@pfmg2025.fr)
Liste des abstracts recensés aux 13èmes Assises
Retrouvez en vidéo l’audition publique organisée par l’OPECST au Sénat le 5 février 2026, consacrée aux enjeux et aux défis des tests génétiques en santé. Une occasion unique d’explorer les avancées médicales, les questions éthiques et les perspectives d’avenir pour une médecine toujours plus personnalisée et responsable.
Sur www.genomecad.fr, vous pourrez désormais :
- Comprendre le rôle et les missions du CAD.
- Explorer les projets déposés et validés par le Comité Scientifique et Éthique (CSE).
- Mieux connaître ses droits concernant la réutilisation de ses données et la manière concrète de les exercer.
- Découvrir la plateforme de données du CAD, son fonctionnement et la procédure d’accès pour les professionnels de la recherche et de la santé.
- Suivre l’actualité du CAD et de ses partenaires.
Comme annoncé dans la dernière lettre d’information (octobre 2025), les travaux menés par l’inspection générale des affaires sociales (IGAS), l’inspection générale de l’éducation, du sport et de la recherche (IGESR) et trois personnalités qualifiées se poursuivent, avec un double volet – évaluation du PFMG et perspectives pour un nouveau plan.
Les ministères en charge de la santé et de la recherche attendent d’ici la fin du mois de mars la remise d’un rapport conjoint qui servira de base à la structuration de l’avenir du plan.

Le Plan France Médecine Génomique 2025 s’attache à garantir un accès équitable à la médecine génomique sur l’ensemble du territoire. Parmi les piliers de ce plan, les Chargé-e-s de Parcours Génomique (CPG) jouent un rôle central. Leur mission ? Faciliter, former et accompagner les professionnels de santé tout au long du parcours de soins génomique.
Le poste de CPG a été initialement créé en 2020, dans le cadre du Plan National Maladies Rares 3. Son succès a conduit à une généralisation en 2022, avec le financement de 51 postes par la Direction Générale de l’Offre de Soins (DGOS), couvrant l’ensemble des préindications du PFMG2025 dans le champ des maladies rares, de l’oncogénétique et des cancers. Leur champ d’action s’étend bien au-delà de la simple aide à la prescription : ils forment les prescripteurs à l’utilisation des outils de e-prescription, participent aux Réunions de Concertation Pluridisciplinaires (RCP-FMG), et organisent les circuits logistiques au niveau local. Pour les CPG également conseillers en génétique, vient s’ajouter l’accompagnement des patients et de leurs familles.
Leur présence sur tout le territoire métropolitain et ultra-marin permet de garantir une couverture homogène et de répondre aux besoins spécifiques des prescripteurs, qu’ils soient en milieu hospitalier ou libéral. Leur rôle est d’autant plus crucial que la médecine génomique repose sur des technologies complexes, nécessitant une formation continue et un accompagnement personnalisé.
Les CPG contribuent également à la mise en place des nouvelles préindications cliniques, en collaboration avec les professionnels de santé et les laboratoires de séquençage, SeqOIA et AURAGEN. Leur action permet d’assurer une transition fluide vers une médecine plus personnalisée, tout en garantissant la qualité et la sécurité des parcours de soins.
Une étude récente, publiée dans European Journal of Human Genetics, dresse un premier bilan de ce dispositif. Menée auprès de 36 CPG sur les 40 en poste au moment de l’étude, l’enquête révèle que la présence de ces professionnels dans les centres de soins permet de fluidifier les parcours, de réduire les délais et d’améliorer la qualité des prescriptions pour toutes les préindications.
Les CPG ont su s’imposer comme des acteurs incontournables, avec une satisfaction professionnelle élevée : 55 % souhaiteraient poursuivre leur mission au-delà des trois ans initialement prévus. Cependant, des défis persistent, comme les contraintes géographiques (logistique des prélèvements, mobilité des patients) ou la nécessité d’harmoniser les pratiques entre les territoires. L’étude souligne également l’importance d’une formation continue, notamment en génomique et en coordination de projets, pour renforcer leurs compétences et leur autonomie.
En novembre 2025, la première Journée Nationale des Chargés de Parcours Génomique a réuni une majorité des CPG à Paris, ainsi que certains participants en visioconférence. Organisée sous l’égide du Groupe de Travail Formation du PFMG2025, cette journée a permis de partager les bonnes pratiques en vue d’harmoniser les processus et de renforcer la collaboration entre les CPG des deux LBM-FMG. Les participants ont souligné l’importance de ces rencontres pour réduire l’isolement géographique et créer une dynamique collective. Comme l’a résumé un CPG lors de l’événement : « Cette journée nous a permis de réaliser que nous faisons face aux mêmes défis et que nos solutions peuvent inspirer nos collègues. C’est un accélérateur de cohésion et d’efficacité. » Les très nombreux sujets du programme de cette première Journée n’ayant pu être assez approfondis d’après les participants, une deuxième édition pour développer les échanges et les interactions est vivement espérée par tous.

Avec plus de 58 000 prescriptions traitées depuis le début du plan, les CPG ont démontré leur valeur ajoutée dans l’implémentation de la médecine génomique. Leur rôle, unique en Europe, pourrait inspirer d’autres pays confrontés aux mêmes enjeux de coordination et d’équité territoriale. En France, la poursuite de ce dispositif constitue un des enjeux majeurs pour la suite du PFMG.
Mme M, patiente de 71 ans, est prise en charge en 2020 pour un carcinome canalaire infiltrant de grade II du sein droit, surexprimant les récepteurs aux oestrogènes (RO+) sans surexpression des récepteurs à la progestérone (RP-), ERBB2 (HER2) non amplifié, traitée par mastectomie puis hormonothérapie par Létrozole. Par ailleurs, elle présentait depuis 2016, un nodule parenchymateux pulmonaire lobaire supérieur gauche d’évolution très lente, non biopsiable, non opérable, qui a été finalement irradié, également en 2020.
En 2022 apparait un nodule sous-cutané para-ombilical gauche pour lequel est effectuée une exérèse. L’examen anatomopathologique retrouve un adénocarcinome infiltrant dont les aspects histologiques et immunohistochimiques ne s’accordent pas avec une origine mammaire, ni clairement avec un autre primitif. Il s’agit donc ici d’un adénocarcinome de primitif inconnu (CUP).
Les explorations secondaires mettent en évidence de multiples lésions dont cérébrales, ganglions cervicaux, pulmonaires et de la sphère ORL. Plusieurs hypothèses cliniques sont retenues dont le carcinome des glandes salivaires ou un adénocarcinome pulmonaire.
Devant ce tableau, le cas est présenté plusieurs fois en RCP nationale CUP avec proposition d’analyse moléculaire dans le cadre du Plan France Médecine Génomique. Une première analyse est effectuée sur le nodule sous-cutané para-ombilical en FFPE, et une nouvelle biopsie d’un nodule cervical gauche accessible est programmée pour disposer d’une analyse plus approfondie sur matériel congelé.
Dans les 2 cas, l’analyse moléculaire retrouve un variant pathogène dans les gènes SETD2, PIK3CA, ARID2, et DNMT2B, ainsi qu’un variant pathogène associé à une perte du deuxième allèle dans le gène STAG2. L’analyse du profil d’expression des gènes, sur tissu congelé par l’outil TransCUPtomics (Vibert et al., 2021) montre que le profil transcriptomique de cette tumeur est compatible avec celui d’un adénocarcinome bronchique (Figure 1).
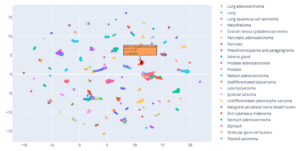
Figure 1: Résultat TransCUPtomics
Au cours de la RCP nationale CUP d’aval, l’ensemble des données moléculaires, cliniques et immunohistochimiques sont confrontées et les expertises réunies à cette RCP tranchent pour une origine pulmonaire de cette tumeur. Ce résultat conforte le traitement envisagé par Carboplatine, Taxol et Pembrolizumab, adapté à un contexte de cancer du poumon.
Sous ce traitement, la patiente a présenté une réponse partielle significative, avec une régression nette des adénopathies médiastinales et une quasi-disparition du nodule pré-scapulaire gauche, associées à une stabilité des nodules pulmonaires.
Toutefois, une nouvelle évaluation à 6 mois a mis en évidence une progression tumorale cérébrale et extra-encéphalique ganglionnaire, justifiant la mise en place d’une radiothérapie cérébrale avec une reprise du pembrolizumab en monothérapie.
L’analyse moléculaire, en identifiant la mutation activatrice du gène PIK3CA pourra permettre l’accès à des essais cliniques pan-tumeurs en cas d’évolution.
Ce cas clinique illustre l’apport du séquençage simultané de l’ADN et de l’ARN tumoral dans le cadre du PFMG2025 afin d’obtenir une caractérisation exhaustive de la tumeur permettant une aide au diagnostic et au choix de la stratégie thérapeutique pour les cancers de primitif inconnu.

En 2025, le Plan France Médecine Génomique 2025 (PFMG2025) a poursuivi son déploiement opérationnel, renforçant l’intégration de la médecine génomique dans le parcours de soin des patients. Avec 58 211 prescriptions validées et 44 165 comptes-rendus remis aux prescripteurs depuis l’ouverture des LBM-FMG en 2019, le PFMG2025 confirme son rôle central dans la prise en charge des maladies rares, des cancers et de l’oncogénétique.
La 5ème vague de préindications a permis la validation de 5 nouvelles préindications, 3 extensions de préindication, 2 mises à jour de la stratégie diagnostique concernant la place du séquençage du génome (passage en première intention pour un sous-groupe de patients), et 1 simplification de la définition d’une préindication. Les 5 vagues ont ainsi permis de passer de 14 préindications lors de la première campagne en 2019, à 82 préindications pour cette fin d’année, réparties en 67 pour les maladies rares, 11 pour les cancers et 4 pour l’oncogénétique.
En 2025, 16 998 prescriptions ont été validées, soit une augmentation de 16 % par rapport à 2024. Les maladies rares et l’oncogénétique représentent 81 % des prescriptions, tandis que les cancers en constituent 19 %.
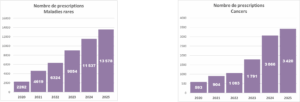
16 632 comptes-rendus ont été remis aux prescripteurs, soit une augmentation de 46 % par rapport à 2024. On constate cette année une augmentation beaucoup plus forte du nombre de comptes-rendus que du nombre de prescriptions, mettant en évidence un effet de rattrapage et une baisse du nombre de dossiers en attente de résultat.
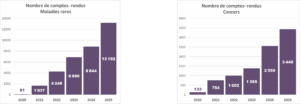
Le CAD, infrastructure clé du PFMG2025, a franchi une étape majeure en 2025 : 5 projets de recherche validés par le Comité Scientifique et Ethique ont vu leurs données transférées vers le HDS Cloud Inserm, permettant l’ouverture de deux premières bulles sécurisées pour les chercheurs.
Les projets pilotes du PFMG2025 poursuivent leurs avancées et ont conduit à la première publication des résultats pour DEFIDIAG (déficience intellectuelle), confirmant l’apport du séquençage du génome complet en trio.
Un manuscrit présentant la mise en œuvre du PFMG2025 et les premiers résultats obtenus dans le cadre du soin a été publié dans Lancet Regional Health Europe au début de l’année 2025 sous une bannière commune rassemblant plus de 1000 contributeurs.
135 articles liés au PFMG2025 ont été recensés dans PubMed en 2025, dont 81 % concernent les maladies rares. Ces travaux contribuent à enrichir les connaissances sur les variants génétiques et leur implication dans différentes maladies, en s’appuyant notamment sur des cohortes internationales de patients. Ils présentent également des protocoles innovants.
Les postes de chargés de parcours génomique sont prolongés pour une durée de 12 mois, renouvelable, facilitant l’accompagnement des prescripteurs et des patients.
23 formations, initiales ou continues, sont désormais référencées par le groupe de travail Formation sur le site du PFMG2025, à l’attention des biologistes, cliniciens, bioinformaticiens et conseillers en génétique.
Le PFMG2025 s’inscrit toujours dans une dynamique européenne, avec une participation active à l’initiative 1+Million Genomes pour le partage des données génomiques au niveau européen, avec le CAD, le CEA et l’Inserm. Il est partenaire des projets Genome of Europe, pour séquencer 100 000 génomes représentatifs des populations européennes, et Genomic Data Infrastructure, pour la mise en place d’une infrastructure fédérée pour le partage des données. Il participe également à la Joint Action Cancer Personalised Medicine qui vient d’être lancée en fin de l’année 2025 pour renforcer la médecine de précision en cancérologie.
En juillet 2025, un accord de collaboration a été signé avec la Hartwig Medical Foundation aux Pays-Bas pour faciliter le partage d’expériences.
Le PFMG2025 a ainsi montré sa capacité à s’adapter aux besoins des patients et des professionnels de la santé et de la recherche, tout en posant les bases d’une médecine génomique confirmée et efficace. Alors qu’il s’achève, les ministères en charge de la santé et de la recherche ont lancé au cours de l’année 2025 des travaux pour évaluer le PFMG et préparer la suite. L’inspection générale des affaires sociales (IGAS), l’inspection générale de l’éducation, du sport et de la recherche (IGESR) et trois personnalités doivent remettre un rapport aux ministères au mois de mars 2026.
Médecine et procréation, dons et transplantation d’organes, neurosciences et neurotechnologies, tests génétiques et médecine génomique… Ces sujets, au cœur de nos vies et de nos sociétés, méritent d’être discutés ensemble.
Pour faciliter votre participation, l’Espace éthique Île-de-France lance un mini-site dédié : un outil clair et accessible pour explorer les thématiques qui vous concernent, consulter notre agenda, vous inscrire aux événements et accéder à des ressources exclusives.
🔹 Trouvez la thématique qui vous interpelle
🔹 Inscrivez-vous aux événements
🔹 Accédez à des ressources en libre accès
En quelques clics, informez-vous et rejoignez le débat citoyen !
Découvrez le mini-site dès maintenant : espace-ethique-egb2026.com
L’initiative européenne « 1+ Million Genome » (1+MG) est un accord entre 25 pays de l’UE et la Norvège visant à permettre un accès transfrontalier sécurisé aux données génomiques (séquençage d’ADN) d’au moins un million d’individus à travers l’Europe. L’accès à ces données est essentiel pour la recherche, le diagnostic précis et le traitement d’un large éventail de maladies génétiques. Les objectifs de l’initiative 1+MG sont coordonnés et financés par des projets tels que l’Infrastructure de données génomiques (GDI). Le projet international « Génome de l’Europe » (GoE), qui vise à constituer une vaste base de données de référence d’informations génétiques issues de populations saines, constitue également un volet important du consortium 1+MG.
Les vidéos suivantes présentent l’initiative 1+MG et ses avantages, et résument les informations clés qui permettront aux citoyens et aux professionnels de santé de mieux comprendre le concept 1+MG.
« Genomics for Everyone » : Comment l’initiative « 1+Million Genomes » profite aux citoyens de l’UE
L’initiative « 1+Million Genomes » (1+MG) vise à garantir que chaque citoyen de l’UE puisse bénéficier des avantages de la génomique, grâce à de meilleurs diagnostics, des traitements ciblés et une prévention améliorée des maladies.
« Genomic Data Is Transforming Patient Care: The 1+MG Initiative Explained »
Cette vidéo destinée aux professionnels de santé explique le rôle clé de l’initiative 1+MG dans le développement de la médecine personnalisée en Europe et l’importance de la collaboration. La Dre Tuula Helander, présidente du groupe 1+MG, déclare : « Sans connaissance des données génomiques, il est impossible d’atteindre l’objectif de la médecine personnalisée. C’est pourquoi nous avons besoin d’une quantité considérable de données et d’une étroite collaboration avec d’autres pays. »
« How Europe Is Unlocking Genomic Data for Personalised Healthcare: The 1+MG Project »
Dans cette vidéo destinée au grand public et aux décideurs, les participants évoquent des exemples de leurs pays d’origine pour expliquer l’importance de la collaboration en vue de trouver une solution commune à l’échelle européenne. En effet, l’initiative 1+MG accélère les avancées scientifiques, soutient les traitements personnalisés et améliore la prévention des maladies en permettant aux chercheurs et aux cliniciens d’étudier les données provenant de tous les États membres de l’UE.
Des essais cliniques récents ont montré que les traitements guidés par la biologie moléculaire peuvent améliorer la survie des patients atteints d’un cancer d’origine inconnue (CUP, Cancer of Unknown Primary). Bien que les CUP ne représentent que 2 à 5 % de toutes les tumeurs malignes, elles constituent la quatrième cause de mortalité liée au cancer en raison de leur pronostic très défavorable. Jusqu’à 85 % des patients atteints d’un CUP appartiennent à un sous-groupe dont le pronostic est défavorable, caractérisé par une survie globale médiane inférieure à un an. La prise en charge standard de ce groupe consiste en une chimiothérapie empirique non spécifique et n’a pas évoluée au cours des dernières décennies. Cependant, la faisabilité et le bénéfice clinique de ces traitements pour les CUP dans la pratique restent incertains.
En France, une Réunion de Concertation Pluridisciplinaire nationale dédiée aux patients atteints de CUP (RCP-CUP) a été créé en 2020, afin de coordonner les analyses diagnostiques pathologiques, cliniques et moléculaires et de fournir une expertise centralisée pour l’orientation diagnostique et thérapeutique des patients. En effet, les progrès récents de la médecine de précision fondée sur le profilage moléculaire ont amélioré la capacité à déterminer le cancer primaire responsable ou à identifier les altérations moléculaires ciblables pour un traitement chez les patients atteints d’un CUP.
Cette RCP a lieu toutes les semaines de manière virtuelle et est composée de pathologistes, biologistes moléculaires et cliniciens, radiologues, répartis sur l’ensemble du territoire. Tout médecin souhaitant adresser le dossier d’un patient pour question sur la prise en charge peut présenter le cas de son ou sa patient(e). L’étude qui visait à évaluer l’impact diagnostique et thérapeutique de cette RCP sur les patients atteints de CUP dans un contexte national réel, vient de voir ses résultats publiés dans The Lancet Regional Health- Europe.
Les caractéristiques des patients et de leurs tumeurs, les traitements et les données de suivi de réponses aux traitements ont été recueillis de manière prospective, pour tous les patients discutés au sein de la RCP-CUP entre juillet 2020 et décembre 2023. L’impact diagnostique de la RCP a été défini comme l’identification d’un tissu d’origine putatif, et l’impact thérapeutique comme le début d’un traitement orienté soit sur l’origine identifiée, soit sur la base d’une cible moléculaire. La survie globale des patients a également été estimée et celle des patients recevant un traitement spécifique orienté grâce aux analyses de la RCP a été comparée à celle des patients recevant un traitement empirique non spécifique.
Au total, 246 patients atteints d’un CUP ont été discutés en RCP-CUP (124 femmes et 122 hommes) entre 2020 et 2023. Un tissu d’origine probable a été identifié chez 70 % des patients entièrement caractérisés, et des altérations moléculaires ciblables ont été trouvées chez 59 % d’entre eux. Les résultats montrent surtout que les recommandations thérapeutiques des experts de la RCP ont conduit à une amélioration cliniquement significative de la survie globale chez les patients traités en fonction des recommandations de la RCP par rapport au traitement empirique standard (18,6 mois vs 11 mois de survie médiane). Cette étude confirme que la médecine de précision pour les CUP est réalisable et efficace en dehors du cadre des essais cliniques, même dans une population hétérogène et à haut risque.
« Notre étude souligne l’urgence de passer d’une logique “un traitement pour tous” à une approche personnalisée adaptée au profil de la maladie. En d’autres termes : chaque patient atteint de CUP mérite une investigation approfondie accessible via la RCP nationale » explique Sarah Watson, porteuse de l’étude. Ces conclusions fournissent en effet une justification solide pour la mise en œuvre à grande échelle de RCP dédiées pour les patients atteints de CUP. La centralisation de l’évaluation pathologique et moléculaire garantit un accès équitable aux outils d’oncologie de précision et améliore à la fois le rendement diagnostique et les résultats en termes de survie.
Par conséquent, les décideurs politiques et les systèmes de santé devraient donner la priorité à l’accès à des discussions multidisciplinaires d’experts, des analyses moléculaires, pathologiques, et cliniques par des établissements référents dès le début du parcours diagnostique des CUP. Des recherches supplémentaires sont nécessaires pour optimiser les délais d’exécution, élargir l’accès aux thérapies ciblées et évaluer de manière prospective la rentabilité de ces stratégies nationales, mais la collaboration multidisciplinaire, le partage des données entre centres, et la mise en place d’un réseau d’expertise dédié à ces cancers se sont déjà révélés concluants.
Références :
Management and survival of patients with cancer of unknown primary discussed by a French national multidisciplinary tumour board: a retrospective analysis
- Dupain et al, The Lancet Regional Health – Europe, 2026
DOI: 10.1016/j.lanepe.2025.101524
French national multidisciplinary tumor board improves the management and survival of patients with cancer of unknown primary (ESMO 2025 poster 3017P)
- Watson et al, Annals of Oncology, Volume 36, Supplement 2, 2025
DOI: 10.1016/j.annonc.2025.08.3632.
Pour aller plus loin :
Communiqué de presse de l’Institut Curie
Article du Quotidien du Médecin

