En 2022, la troisième campagne de validation de nouvelles préindications mise en œuvre par un groupe de travail piloté par la HAS a conduit à la
validation de 9 nouvelles préindications dans le domaine des maladies rares et de 2 extensions de préindications en cancérologie. Au total, il est aujourd’hui possible de prescrire un examen pangénomique pour
70 préindications, dont 60 dans le champ des maladies rares, 8 en cancérologie et 2 en oncogénétique.
Par ailleurs, plusieurs actions ont été menées l’an dernier afin de faciliter le parcours de soin :
-
- En particulier, 51 postes de chargés de parcours génomique ont été déployés pour toutes les préindications du PFMG2025. Ils bénéficient d’un financement de la DGOS pour une durée de 3 ans qui élargit ainsi la mesure initiale menée dans le cadre du PNMR3. Répartis sur l’ensemble du territoire, les chargés de parcours génomique sont en charge de former et d’accompagner les prescripteurs, de contribuer à mettre en place au niveau local, puis à fluidifier, les parcours de soins des différentes préindications.
- Dans le champ des maladies rares, des RCP-FMG-MR Génomiques ont été mises en place sur l’ensemble du territoire à l’issue d’une phase pilote de 6 mois. Ces RCP-FMG plurithématiques permettent de valider la prescription d’un séquençage pangénomique pour l’ensemble des préindications maladies rares quand la situation médicale du patient respecte des critères phénotypiques de prescription, conduisant ainsi à une simplification du parcours de soins.
- En cancérologie, deux phases pilotes ont été mises en œuvre pour envisager l’utilisation de prélèvements fixés (FFPE) et d’ADN tumoral circulant. Les résultats sont attendus en 2023 et conduiront à définir les modalités de recours aux différents types de prélèvements selon les préindications.
 Chaque mois, les LBM-FMG SeqOIA et AURAGEN transmettent un bilan d’activité à l’équipe de coordination du PFMG qui en fait une synthèse à l’échelle nationale.
7 387 prescriptions ont été validées en RCP-FMG d’amont en 2022
Chaque mois, les LBM-FMG SeqOIA et AURAGEN transmettent un bilan d’activité à l’équipe de coordination du PFMG qui en fait une synthèse à l’échelle nationale.
7 387 prescriptions ont été validées en RCP-FMG d’amont en 2022 :
- 6 255 pour les maladies rares
- 69 pour l’oncogénétique
- 1 063 pour les cancers
Et 5 250 comptes rendus ont été remis aux médecins prescripteurs :
- 4 248 pour les maladies rares
- 1 002 pour les cancers
Ainsi, plus de 15 000 prescriptions ont été effectuées et plus de 7800 comptes-rendus ont été remis aux prescripteurs dans le cadre du PFMG2025.
L’implication forte de nombreux acteurs du parcours de soin se traduit en 2022 par la poursuite de la dynamique de montée en charge de l’activité par rapport aux années précédentes, tant par l’augmentation du nombre de prescriptions (+33,7%) que par le nombre de comptes-rendus remis aux prescripteurs (x2,2). En particulier, l’augmentation très significative du nombre de comptes-rendus en 2022 illustre la mobilisation des biologistes pour l’interprétation clinico-biologique, un des enjeux majeurs du PFMG2025.
Néanmoins, les efforts doivent se poursuivre, en particulier pour augmenter le nombre de prescriptions dans le champ des cancers et réduire le délai de rendu des résultats dans le champ des maladies rares.
-
Les projets pilotes du PFMG2025
Menés dans le cadre de la recherche,
les projets pilotes visent à identifier les différents verrous d’ordre technologique, réglementaire et organisationnel au niveau du parcours de soin. Ils comprennent également des projets ancillaires dans le champ des Sciences Humaines et Sociales et d’évaluation médico-économique.
-
- Les inclusions dans le projet DEFIDIAG, portant sur la déficience intellectuelle, se sont achevées en avril 2022. 1275 trios ont été inclus et les résultats de séquençage sont en cours d’analyse.
- 344 patients ont été randomisés dans l’essai MULTISARC, portant sur les sarcomes, avec un accès possible ensuite à 10 thérapies ciblées dans le cadre de l’essai clinique. Les inclusions dans le bras olaparib/durvalumab ont été suspendues en novembre 2022, le nombre requis de patients ayant été atteint.
- Les inclusions dans le projet en population générale POPGEN sont terminées, avec plus de 10000 participants de la cohorte Constance. Les génotypages sont achevés et le séquençage du génome de 4000 de ces participants est en cours.
- Le protocole de GLUCOGEN, portant sur le diabète, est finalisé et sera soumis très prochainement aux autorités réglementaires.
-
La réutilisation des données pour la recherche
Le Collecteur Analyseur de Données (CAD) est l’infrastructure du PFMG2025 permettant la réutilisation des données du PFMG2025 dans le cadre de la recherche.
-
- 8 projets de recherche ont déposé une demande d’accès aux données auprès du Comité Scientique et Ethique (CSE) du CAD, 5 dans le champ des maladies rares et 3 en cancérologie,
- 5 demandes d’accès aux données sont en cours d’évaluation,
- et 3 projets de recherche ont été validés par le CSE.
Une étape majeure pour le Collecteur Analyseur de Données du PFMG2025
Le PFMG2025 a comme ambition d’intégrer la médecine génomique dans le parcours de soins des patients. 70 préindications ont été validées à ce jour (60 préindications pour les maladies rares, 2 pour l’oncogénétique et 8 en cancérologie) et ont conduit à la prescription d’un examen pangénomique pour
15 000 patients.
Les données génomiques produites par
les laboratoires LBM-FMG SeqOIA et AURAGEN ainsi que celles provenant des
quatre projets pilotes du PFMG2025 (
DEFIDIAG pour la déficience intellectuelle,
MULTIPLI pour les sarcomes des tissus mous,
POPGEN en population générale et
GLUCOGEN pour les formes atypiques du diabète) ont vocation à alimenter
le Collecteur Analyseur de Données (CAD), constituant ainsi une ressource nationale de données génomiques et de données cliniques associées.
Plus de 7800 comptes-rendus ont été remis aux prescripteurs, dont quasiment 6000 pour des patients atteints de maladies rares et 1900 pour des patients atteints de cancers. Ainsi, les données génomiques et cliniques de 7800 patients, et le cas échéant de membres de leur famille, sont d’ores et déjà accessibles pour la recherche. L’accès aux données de DEFIDIAG et de MULTISARC est également possible sous certaines conditions tant que ces deux essais cliniques sont encore en cours.
En y associant une puissance de calcul adaptée et un éventail d’outils informatiques au sein d’une infrastructure dédiée,
le CAD permet d’inscrire le PFMG2025 dans un continuum entre le soin et la recherche, au bénéfice des patients. Il proposera ainsi des services pour le soin et la recherche :
- Dans le cadre du soin, il fournira aux praticiens des outils contribuant à l’interprétation clinico-biologique des données individuelles, ainsi qu’à leur réanalyse dans la poursuite de la démarche diagnostique ;
- Dans le cadre de la recherche, il mettra à disposition des chercheurs les données collectées dans le cadre du soin pour produire de nouvelles connaissances.
Également à l’interface entre le soin et la recherche, le CAD met en œuvre la base de connaissances nationale « FMG-kb », alimentée par les données du PFMG2025, dont l’objet sera de faciliter l’analyse, la réanalyse et le partage des variations d’intérêt dans le cadre du soin comme de la recherche. Un groupe de travail, composé de cliniciens, de biologistes et de bioformaticiens est actuellement en charge de définir les fonctionnalités attendues.
Le CAD sera hébergé dans 2 des 4 centres de calcul nationaux : le Centre Informatique National de l’Enseignement Supérieur, à Montpellier, et le Très Grand Centre de Calcul du CEA, en Ile-de-France.
Une nouvelle étape a été franchie récemment pour le CAD : la
publication du groupement d’intérêt public « Collecteur Analyseur de Données » au Journal Officiel. La première assemblée générale du GIP va réunir prochainement les 9 membres fondateurs (l’Etat (MESR et MSP), Auragen, SeqOIA, le CEA, France Universités, la Conférence des DG de CHU, l’Inria, l’Inserm, Unicancer), ce qui permettra d’accélérer sa mise en œuvre.
Les premiers services opérationnels concerneront le volet recherche.
Une procédure d’accès aux données a été définie, avec la mise en place d’un Comité Scientifique et Ethique (CSE) multidisciplinaire en charge de valider les demandes d’accès aux données génomiques des chercheurs et d’un guichet d’accompagnement permettant d’expliquer et de faciliter les démarches.
Après validation du CSE, les données du PFMG2025 nécessaires au projet seront mises à disposition de l’équipe de recherche au sein d’une bulle sécurisée dédiée, excluant la possibilité de copie ou d’extraction des données identifiantes. Les chercheurs pourront disposer aussi d’outils d’analyse et de la capacité de calcul nécessaire. En outre, ils auront la possibilité d’importer dans cette même bulle sécurisée leurs propres outils d’analyse et données. Ils pourront ainsi mener leur projet de recherche dans un environnement qui leur sera réservé, garantissant ainsi à la fois la sécurité des données et la confidentialité de leurs travaux.
A ce jour, 5 demandes d’accès aux données sont en cours d’évaluation et
3 projets de recherche ont été validés par le CSE. L’infrastructure du CAD se déploie progressivement. Des bulles sécurisées sont opérationnelles pour ces projets, permettant d’envisager les premières mises à disposition des données du PFMG2025 au cours de ce trimestre.
Par ailleurs, le CAD s’inscrit dans une
dynamique européenne, notamment au travers de l’initiative 1+ Million Genomes à laquelle la France a adhéré récemment, en lien étroit avec le PFMG2025. En particulier, le CAD participe au projet européen Genomic Data Infrastructure visant à mettre en œuvre le partage des données génomiques à l’échelle européenne. Ainsi, les données génomiques du PFMG2025 pourront être mises à disposition à l’échelle européenne et les chercheurs français pourront accéder à celles produites dans les autres pays.
Cas clinique : Une surdité neurosensorielle congénitale
Un nourrisson est reçu en consultation de Génétique à Limoges dans les suites du diagnostic d’une surdité neurosensorielle congénitale dépistée à la naissance.
Deuxième enfant de parents non apparentés sans antécédent familial particulier, il présente une surdité bilatérale sévère à profonde, isolée, sans malformation au scanner des rochers et à l’IRM cérébrale. Cet enfant a rapidement bénéficié de la pose d’implants cochléaires. Toutefois l’évolution montre un retard de développement et d’acquisition de la marche, avec un questionnement sur d’éventuels traits autistiques. Cet enfant présente quelques particularités morphologiques avec un grand front bombé, une dystopie des canthi, une racine du nez large et une ensellure nasale marquée, à pondérer par l’origine ethnique. Ses mensurations (Taille, Poids et PC) sont dans les normes.
Les premiers bilans génétiques (analyse de
DFNB1, ACPA, panel de gènes impliqués dans les surdités)
reviennent sans anomalie, de même que la sérologie CMV.
L’indication de séquençage du génome est alors retenue par
la RCP nationale de la filière SENSGENE. Une analyse
en trio (cas index et 2 parents) est réalisée dans
le laboratoire AURAGEN.
Deux variations génétiques sont identifiées en trans dans le gène CDH23 :
- une variation faux-sens, p.(Arg1746Gln), hérité du père, considéré comme pathogène, déjà été rapporté dans la littérature chez des patients porteurs d’un syndrome de Usher,
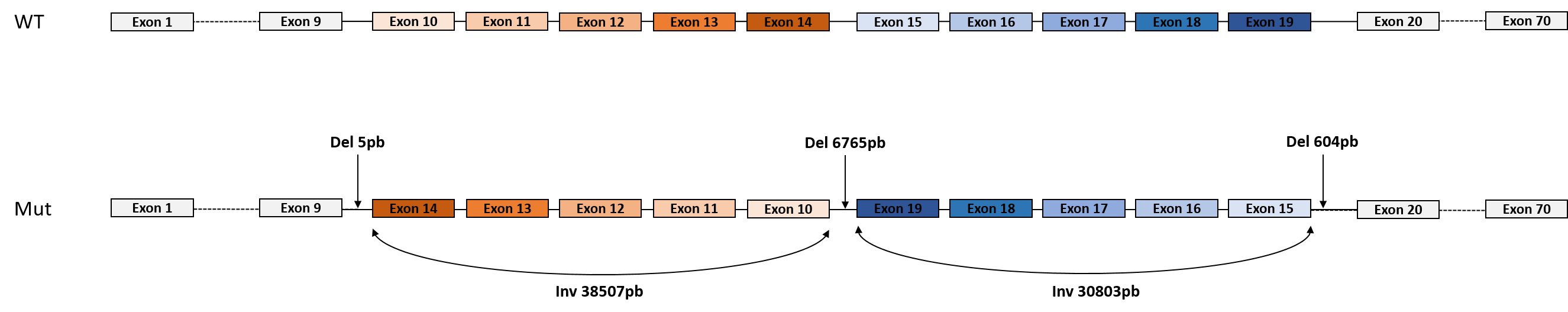
- un remaniement chromosomique complexe, hérité de la mère. Il s’agit de deux inversions côte à côte, intragéniques et associées à trois délétions introniques de part et d’autre et entre les deux inversions (cf figure). La conséquence de ce remaniement complexe est vraisemblablement pathogène et équivalente à un allèle nul. Les outils bio-informatiques du laboratoire AURAGEN ont détecté les deux inversions, mais seule la visualisation et l’analyse sur IGV par les soft-clip a permis de voir et de préciser les délétions.
Le gène
CDH23 est impliqué dans le syndrome de Usher de type 1 et dans la surdité non syndromique, de transmission autosomique récessive. Le syndrome de Usher de type 1 est défini par l’association d’une surdité congénitale sévère à profonde, d’une rétinopathie pigmentaire au cours de la première décade et dans la majorité des cas d’une aréfléxie vestibulaire se traduisant notamment par un retard d’acquisition de la marche.
Un phénotypage inverse pour corréler ces données génomiques aux données cliniques est en cours avec en particulier un examen ophtalmologique pour déterminer si cet enfant présente une rétinopathie pigmentaire associée à sa surdité. Il est compliqué à ce stade de donner un pronostic car même en absence de rétinopathie pigmentaire, étant donné le jeune âge du patient, on ne peut exclure l’apparition de signes ophtalmologiques plus tardifs.
Le diagnostic de syndrome de Usher à partir d’une surdité a priori isolée est utile pour adapter la prise en charge de la personne et donner un conseil génétique adéquat.
Le séquençage du génome a permis d’apporter une explication à la surdité de cet enfant alors que les analyses classiques antérieures ne l’avaient pas permis. Les outils bioinformatiques développés par
le laboratoire AURAGEN ont en effet permis d’identifier un remaniement chromosomique complexe intragénique, non détecté par l’ACPA.
Même s’ils restent une cause minoritaire dans les pathologies monogéniques, les remaniements chromosomiques doivent être recherchés.
Le laboratoire AURAGEN a d’autres exemples similaires de remaniements de petite taille ou d’allure équilibrée, impliqués dans les pathologies monogéniques.


 Chaque mois,
Chaque mois,  En y associant une puissance de calcul adaptée et un éventail d’outils informatiques au sein d’une infrastructure dédiée, le CAD permet d’inscrire le PFMG2025 dans un continuum entre le soin et la recherche, au bénéfice des patients. Il proposera ainsi des services pour le soin et la recherche :
En y associant une puissance de calcul adaptée et un éventail d’outils informatiques au sein d’une infrastructure dédiée, le CAD permet d’inscrire le PFMG2025 dans un continuum entre le soin et la recherche, au bénéfice des patients. Il proposera ainsi des services pour le soin et la recherche :
 Le gène CDH23 est impliqué dans le syndrome de Usher de type 1 et dans la surdité non syndromique, de transmission autosomique récessive. Le syndrome de Usher de type 1 est défini par l’association d’une surdité congénitale sévère à profonde, d’une rétinopathie pigmentaire au cours de la première décade et dans la majorité des cas d’une aréfléxie vestibulaire se traduisant notamment par un retard d’acquisition de la marche.
Un phénotypage inverse pour corréler ces données génomiques aux données cliniques est en cours avec en particulier un examen ophtalmologique pour déterminer si cet enfant présente une rétinopathie pigmentaire associée à sa surdité. Il est compliqué à ce stade de donner un pronostic car même en absence de rétinopathie pigmentaire, étant donné le jeune âge du patient, on ne peut exclure l’apparition de signes ophtalmologiques plus tardifs.
Le diagnostic de syndrome de Usher à partir d’une surdité a priori isolée est utile pour adapter la prise en charge de la personne et donner un conseil génétique adéquat.
Le séquençage du génome a permis d’apporter une explication à la surdité de cet enfant alors que les analyses classiques antérieures ne l’avaient pas permis. Les outils bioinformatiques développés par
Le gène CDH23 est impliqué dans le syndrome de Usher de type 1 et dans la surdité non syndromique, de transmission autosomique récessive. Le syndrome de Usher de type 1 est défini par l’association d’une surdité congénitale sévère à profonde, d’une rétinopathie pigmentaire au cours de la première décade et dans la majorité des cas d’une aréfléxie vestibulaire se traduisant notamment par un retard d’acquisition de la marche.
Un phénotypage inverse pour corréler ces données génomiques aux données cliniques est en cours avec en particulier un examen ophtalmologique pour déterminer si cet enfant présente une rétinopathie pigmentaire associée à sa surdité. Il est compliqué à ce stade de donner un pronostic car même en absence de rétinopathie pigmentaire, étant donné le jeune âge du patient, on ne peut exclure l’apparition de signes ophtalmologiques plus tardifs.
Le diagnostic de syndrome de Usher à partir d’une surdité a priori isolée est utile pour adapter la prise en charge de la personne et donner un conseil génétique adéquat.
Le séquençage du génome a permis d’apporter une explication à la surdité de cet enfant alors que les analyses classiques antérieures ne l’avaient pas permis. Les outils bioinformatiques développés par