
En 2025, le Plan France Médecine Génomique 2025 (PFMG2025) a poursuivi son déploiement opérationnel, renforçant l’intégration de la médecine génomique dans le parcours de soin des patients. Avec 58 211 prescriptions validées et 44 165 comptes-rendus remis aux prescripteurs depuis l’ouverture des LBM-FMG en 2019, le PFMG2025 confirme son rôle central dans la prise en charge des maladies rares, des cancers et de l’oncogénétique.
La 5
ème vague de préindications a permis la validation de 5 nouvelles préindications, 3 extensions de préindication, 2 mises à jour de la stratégie diagnostique concernant la place du séquençage du génome (passage en première intention pour un sous-groupe de patients), et 1 simplification de la définition d’une préindication. Les 5 vagues ont ainsi permis de passer de 14 préindications lors de la première campagne en 2019, à 82 préindications pour cette fin d’année, réparties en 67 pour les maladies rares, 11 pour les cancers et 4 pour l’oncogénétique.
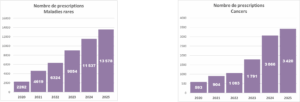
En 2025, 16 998 prescriptions ont été validées, soit une augmentation de 16 % par rapport à 2024. Les maladies rares et l’oncogénétique représentent 81 % des prescriptions, tandis que les cancers en constituent 19 %.
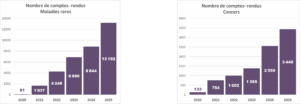
16 632 comptes-rendus ont été remis aux prescripteurs, soit une augmentation de 46 % par rapport à 2024. On constate cette année une augmentation beaucoup plus forte du nombre de comptes-rendus que du nombre de prescriptions, mettant en évidence un effet de rattrapage et une baisse du nombre de dossiers en attente de résultat.
Le CAD, infrastructure clé du PFMG2025, a franchi une étape majeure en 2025 : 5 projets de recherche validés par le Comité Scientifique et Ethique ont vu leurs données transférées vers le HDS Cloud Inserm, permettant l’ouverture de deux premières bulles sécurisées pour les chercheurs.
Les projets pilotes du PFMG2025 poursuivent leurs avancées et ont conduit à la
première publication des résultats pour DEFIDIAG (déficience intellectuelle), confirmant l’apport du séquençage du génome complet en
trio.
Un manuscrit présentant la mise en œuvre du PFMG2025 et les premiers résultats obtenus dans le cadre du soin a été publié dans
Lancet Regional Health Europe au début de l’année 2025 sous une bannière commune rassemblant plus de 1000 contributeurs.
135 articles liés au PFMG2025 ont été recensés dans PubMed en 2025, dont 81 % concernent les maladies rares. Ces travaux contribuent à enrichir les connaissances sur les variants génétiques et leur implication dans différentes maladies, en s’appuyant notamment sur des cohortes internationales de patients. Ils présentent également des protocoles innovants.
Les postes de chargés de parcours génomique sont prolongés pour une durée de 12 mois, renouvelable, facilitant l’accompagnement des prescripteurs et des patients.
23 formations, initiales ou continues, sont désormais référencées par le groupe de travail Formation sur le site du PFMG2025, à l’attention des biologistes, cliniciens, bioinformaticiens et conseillers en génétique.
Le PFMG2025 s’inscrit toujours dans une dynamique européenne, avec une participation active à l’initiative 1+Million Genomes pour le partage des données génomiques au niveau européen, avec le CAD, le CEA et l’Inserm. Il est partenaire des projets Genome of Europe, pour séquencer 100 000 génomes représentatifs des populations européennes, et Genomic Data Infrastructure, pour la mise en place d’une infrastructure fédérée pour le partage des données. Il participe également à la Joint Action Cancer Personalised Medicine qui vient d’être lancée en fin de l’année 2025 pour renforcer la médecine de précision en cancérologie.
En juillet 2025, un accord de collaboration a été signé avec la Hartwig Medical Foundation aux Pays-Bas pour faciliter le partage d’expériences.
Le PFMG2025 a ainsi montré sa capacité à s’adapter aux besoins des patients et des professionnels de la santé et de la recherche, tout en posant les bases d’une médecine génomique confirmée et efficace. Alors qu’il s’achève, les ministères en charge de la santé et de la recherche ont lancé au cours de l’année 2025 des travaux pour évaluer le PFMG et préparer la suite. L’inspection générale des affaires sociales (IGAS), l’inspection générale de l’éducation, du sport et de la recherche (IGESR) et trois personnalités doivent remettre un rapport aux ministères au mois de mars 2026.
Les Chargé-e-s de Parcours Génomique : des acteurs clés pour optimiser le parcours de soins en médecine génomique
 Le Plan France Médecine Génomique 2025 s’attache à garantir un accès équitable à la médecine génomique sur l’ensemble du territoire. Parmi les piliers de ce plan, les Chargé-e-s de Parcours Génomique (CPG) jouent un rôle central. Leur mission ? Faciliter, former et accompagner les professionnels de santé tout au long du parcours de soins génomique.
Le Plan France Médecine Génomique 2025 s’attache à garantir un accès équitable à la médecine génomique sur l’ensemble du territoire. Parmi les piliers de ce plan, les Chargé-e-s de Parcours Génomique (CPG) jouent un rôle central. Leur mission ? Faciliter, former et accompagner les professionnels de santé tout au long du parcours de soins génomique.
Le poste de CPG a été initialement créé en 2020, dans le cadre du Plan National Maladies Rares 3. Son succès a conduit à une généralisation en 2022, avec le financement de 51 postes par la Direction Générale de l’Offre de Soins (DGOS), couvrant l’ensemble des préindications du PFMG2025 dans le champ des maladies rares, de l’oncogénétique et des cancers. Leur champ d’action s’étend bien au-delà de la simple aide à la prescription : ils forment les prescripteurs à l’utilisation des outils de e-prescription, participent aux Réunions de Concertation Pluridisciplinaires (RCP-FMG), et organisent les circuits logistiques au niveau local. Pour les CPG également conseillers en génétique, vient s’ajouter l’accompagnement des patients et de leurs familles.
Leur présence sur tout le territoire métropolitain et ultra-marin permet de garantir une couverture homogène et de répondre aux besoins spécifiques des prescripteurs, qu’ils soient en milieu hospitalier ou libéral. Leur rôle est d’autant plus crucial que la médecine génomique repose sur des technologies complexes, nécessitant une formation continue et un accompagnement personnalisé.
Les CPG contribuent également à la mise en place des nouvelles préindications cliniques, en collaboration avec les professionnels de santé et les laboratoires de séquençage, SeqOIA et AURAGEN. Leur action permet d’assurer une transition fluide vers une médecine plus personnalisée, tout en garantissant la qualité et la sécurité des parcours de soins.
Une étude récente, publiée dans
European Journal of Human Genetics, dresse un premier bilan de ce dispositif. Menée auprès de 36 CPG sur les 40 en poste au moment de l’étude, l’enquête révèle que la présence de ces professionnels dans les centres de soins permet de fluidifier les parcours, de réduire les délais et d’améliorer la qualité des prescriptions pour toutes les préindications.
Les CPG ont su s’imposer comme des acteurs incontournables, avec une satisfaction professionnelle élevée : 55 % souhaiteraient poursuivre leur mission au-delà des trois ans initialement prévus. Cependant, des défis persistent, comme les contraintes géographiques (logistique des prélèvements, mobilité des patients) ou la nécessité d’harmoniser les pratiques entre les territoires. L’étude souligne également l’importance d’une formation continue, notamment en génomique et en coordination de projets, pour renforcer leurs compétences et leur autonomie.
En novembre 2025, la première Journée Nationale des Chargés de Parcours Génomique a réuni une majorité des CPG à Paris, ainsi que certains participants en visioconférence. Organisée sous l’égide du Groupe de Travail Formation du PFMG2025, cette journée a permis de partager les bonnes pratiques en vue d’harmoniser les processus et de renforcer la collaboration entre les CPG des deux LBM-FMG. Les participants ont souligné l’importance de ces rencontres pour réduire l’isolement géographique et créer une dynamique collective. Comme l’a résumé un CPG lors de l’événement :
« Cette journée nous a permis de réaliser que nous faisons face aux mêmes défis et que nos solutions peuvent inspirer nos collègues. C’est un accélérateur de cohésion et d’efficacité. » Les très nombreux sujets du programme de cette première Journée n’ayant pu être assez approfondis d’après les participants, une deuxième édition pour développer les échanges et les interactions est vivement espérée par tous.

Avec plus de 58 000 prescriptions traitées depuis le début du plan, les CPG ont démontré leur valeur ajoutée dans l’implémentation de la médecine génomique. Leur rôle, unique en Europe, pourrait inspirer d’autres pays confrontés aux mêmes enjeux de coordination et d’équité territoriale. En France, la poursuite de ce dispositif constitue un des enjeux majeurs pour la suite du PFMG.
Cas clinique : une patiente avec cancer du sein et nodules multiples
Mme M, patiente de 71 ans, est prise en charge en 2020 pour un carcinome canalaire infiltrant de grade II du sein droit, surexprimant les récepteurs aux oestrogènes (RO+) sans surexpression des récepteurs à la progestérone (RP-),
ERBB2 (HER2) non amplifié, traitée par mastectomie puis hormonothérapie par Létrozole. Par ailleurs, elle présentait depuis 2016, un nodule parenchymateux pulmonaire lobaire supérieur gauche d’évolution très lente, non biopsiable, non opérable, qui a été finalement irradié, également en 2020.
En 2022 apparait un nodule sous-cutané para-ombilical gauche pour lequel est effectuée une exérèse. L’examen anatomopathologique retrouve un adénocarcinome infiltrant dont les aspects histologiques et immunohistochimiques ne s’accordent pas avec une origine mammaire, ni clairement avec un autre primitif. Il s’agit donc ici d’un adénocarcinome de primitif inconnu (CUP).
Les explorations secondaires mettent en évidence de multiples lésions dont cérébrales, ganglions cervicaux, pulmonaires et de la sphère ORL. Plusieurs hypothèses cliniques sont retenues dont le carcinome des glandes salivaires ou un adénocarcinome pulmonaire.
Devant ce tableau, le cas est présenté plusieurs fois en RCP nationale CUP avec proposition d’analyse moléculaire dans le cadre du Plan France Médecine Génomique. Une première analyse est effectuée sur le nodule sous-cutané para-ombilical en FFPE, et une nouvelle biopsie d’un nodule cervical gauche accessible est programmée pour disposer d’une analyse plus approfondie sur matériel congelé.
Dans les 2 cas, l’analyse moléculaire retrouve un variant pathogène dans les gènes
SETD2,
PIK3CA,
ARID2, et
DNMT2B, ainsi qu’un variant pathogène associé à une perte du deuxième allèle dans le gène
STAG2. L’analyse du profil d’expression des gènes, sur tissu congelé par l’outil
TransCUPtomics (
Vibert et al., 2021) montre que le profil transcriptomique de cette tumeur est compatible avec celui d’un adénocarcinome bronchique (Figure 1).
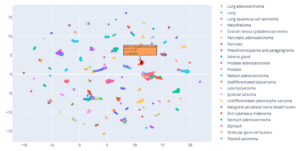
Figure 1: Résultat TransCUPtomics
Au cours de la RCP nationale CUP d’aval, l’ensemble des données moléculaires, cliniques et immunohistochimiques sont confrontées et les expertises réunies à cette RCP tranchent pour une origine pulmonaire de cette tumeur. Ce résultat conforte le traitement envisagé par Carboplatine, Taxol et Pembrolizumab, adapté à un contexte de cancer du poumon.
Sous ce traitement, la patiente a présenté une réponse partielle significative, avec une régression nette des adénopathies médiastinales et une quasi-disparition du nodule pré-scapulaire gauche, associées à une stabilité des nodules pulmonaires.
Toutefois, une nouvelle évaluation à 6 mois a mis en évidence une progression tumorale cérébrale et extra-encéphalique ganglionnaire, justifiant la mise en place d’une radiothérapie cérébrale avec une reprise du pembrolizumab en monothérapie.
L’analyse moléculaire, en identifiant la mutation activatrice du gène
PIK3CA pourra permettre l’accès à des essais cliniques pan-tumeurs en cas d’évolution.
Ce cas clinique illustre l’apport du séquençage simultané de l’ADN et de l’ARN tumoral dans le cadre du PFMG2025 afin d’obtenir une caractérisation exhaustive de la tumeur permettant une aide au diagnostic et au choix de la stratégie thérapeutique pour les cancers de primitif inconnu.


 En 2025, le Plan France Médecine Génomique 2025 (PFMG2025) a poursuivi son déploiement opérationnel, renforçant l’intégration de la médecine génomique dans le parcours de soin des patients. Avec 58 211 prescriptions validées et 44 165 comptes-rendus remis aux prescripteurs depuis l’ouverture des LBM-FMG en 2019, le PFMG2025 confirme son rôle central dans la prise en charge des maladies rares, des cancers et de l’oncogénétique.
La 5ème vague de préindications a permis la validation de 5 nouvelles préindications, 3 extensions de préindication, 2 mises à jour de la stratégie diagnostique concernant la place du séquençage du génome (passage en première intention pour un sous-groupe de patients), et 1 simplification de la définition d’une préindication. Les 5 vagues ont ainsi permis de passer de 14 préindications lors de la première campagne en 2019, à 82 préindications pour cette fin d’année, réparties en 67 pour les maladies rares, 11 pour les cancers et 4 pour l’oncogénétique.
En 2025, 16 998 prescriptions ont été validées, soit une augmentation de 16 % par rapport à 2024. Les maladies rares et l’oncogénétique représentent 81 % des prescriptions, tandis que les cancers en constituent 19 %.
En 2025, le Plan France Médecine Génomique 2025 (PFMG2025) a poursuivi son déploiement opérationnel, renforçant l’intégration de la médecine génomique dans le parcours de soin des patients. Avec 58 211 prescriptions validées et 44 165 comptes-rendus remis aux prescripteurs depuis l’ouverture des LBM-FMG en 2019, le PFMG2025 confirme son rôle central dans la prise en charge des maladies rares, des cancers et de l’oncogénétique.
La 5ème vague de préindications a permis la validation de 5 nouvelles préindications, 3 extensions de préindication, 2 mises à jour de la stratégie diagnostique concernant la place du séquençage du génome (passage en première intention pour un sous-groupe de patients), et 1 simplification de la définition d’une préindication. Les 5 vagues ont ainsi permis de passer de 14 préindications lors de la première campagne en 2019, à 82 préindications pour cette fin d’année, réparties en 67 pour les maladies rares, 11 pour les cancers et 4 pour l’oncogénétique.
En 2025, 16 998 prescriptions ont été validées, soit une augmentation de 16 % par rapport à 2024. Les maladies rares et l’oncogénétique représentent 81 % des prescriptions, tandis que les cancers en constituent 19 %.
 16 632 comptes-rendus ont été remis aux prescripteurs, soit une augmentation de 46 % par rapport à 2024. On constate cette année une augmentation beaucoup plus forte du nombre de comptes-rendus que du nombre de prescriptions, mettant en évidence un effet de rattrapage et une baisse du nombre de dossiers en attente de résultat.
16 632 comptes-rendus ont été remis aux prescripteurs, soit une augmentation de 46 % par rapport à 2024. On constate cette année une augmentation beaucoup plus forte du nombre de comptes-rendus que du nombre de prescriptions, mettant en évidence un effet de rattrapage et une baisse du nombre de dossiers en attente de résultat.
 Le CAD, infrastructure clé du PFMG2025, a franchi une étape majeure en 2025 : 5 projets de recherche validés par le Comité Scientifique et Ethique ont vu leurs données transférées vers le HDS Cloud Inserm, permettant l’ouverture de deux premières bulles sécurisées pour les chercheurs.
Les projets pilotes du PFMG2025 poursuivent leurs avancées et ont conduit à la
Le CAD, infrastructure clé du PFMG2025, a franchi une étape majeure en 2025 : 5 projets de recherche validés par le Comité Scientifique et Ethique ont vu leurs données transférées vers le HDS Cloud Inserm, permettant l’ouverture de deux premières bulles sécurisées pour les chercheurs.
Les projets pilotes du PFMG2025 poursuivent leurs avancées et ont conduit à la  Le Plan France Médecine Génomique 2025 s’attache à garantir un accès équitable à la médecine génomique sur l’ensemble du territoire. Parmi les piliers de ce plan, les Chargé-e-s de Parcours Génomique (CPG) jouent un rôle central. Leur mission ? Faciliter, former et accompagner les professionnels de santé tout au long du parcours de soins génomique.
Le poste de CPG a été initialement créé en 2020, dans le cadre du Plan National Maladies Rares 3. Son succès a conduit à une généralisation en 2022, avec le financement de 51 postes par la Direction Générale de l’Offre de Soins (DGOS), couvrant l’ensemble des préindications du PFMG2025 dans le champ des maladies rares, de l’oncogénétique et des cancers. Leur champ d’action s’étend bien au-delà de la simple aide à la prescription : ils forment les prescripteurs à l’utilisation des outils de e-prescription, participent aux Réunions de Concertation Pluridisciplinaires (RCP-FMG), et organisent les circuits logistiques au niveau local. Pour les CPG également conseillers en génétique, vient s’ajouter l’accompagnement des patients et de leurs familles.
Leur présence sur tout le territoire métropolitain et ultra-marin permet de garantir une couverture homogène et de répondre aux besoins spécifiques des prescripteurs, qu’ils soient en milieu hospitalier ou libéral. Leur rôle est d’autant plus crucial que la médecine génomique repose sur des technologies complexes, nécessitant une formation continue et un accompagnement personnalisé.
Les CPG contribuent également à la mise en place des nouvelles préindications cliniques, en collaboration avec les professionnels de santé et les laboratoires de séquençage, SeqOIA et AURAGEN. Leur action permet d’assurer une transition fluide vers une médecine plus personnalisée, tout en garantissant la qualité et la sécurité des parcours de soins.
Le Plan France Médecine Génomique 2025 s’attache à garantir un accès équitable à la médecine génomique sur l’ensemble du territoire. Parmi les piliers de ce plan, les Chargé-e-s de Parcours Génomique (CPG) jouent un rôle central. Leur mission ? Faciliter, former et accompagner les professionnels de santé tout au long du parcours de soins génomique.
Le poste de CPG a été initialement créé en 2020, dans le cadre du Plan National Maladies Rares 3. Son succès a conduit à une généralisation en 2022, avec le financement de 51 postes par la Direction Générale de l’Offre de Soins (DGOS), couvrant l’ensemble des préindications du PFMG2025 dans le champ des maladies rares, de l’oncogénétique et des cancers. Leur champ d’action s’étend bien au-delà de la simple aide à la prescription : ils forment les prescripteurs à l’utilisation des outils de e-prescription, participent aux Réunions de Concertation Pluridisciplinaires (RCP-FMG), et organisent les circuits logistiques au niveau local. Pour les CPG également conseillers en génétique, vient s’ajouter l’accompagnement des patients et de leurs familles.
Leur présence sur tout le territoire métropolitain et ultra-marin permet de garantir une couverture homogène et de répondre aux besoins spécifiques des prescripteurs, qu’ils soient en milieu hospitalier ou libéral. Leur rôle est d’autant plus crucial que la médecine génomique repose sur des technologies complexes, nécessitant une formation continue et un accompagnement personnalisé.
Les CPG contribuent également à la mise en place des nouvelles préindications cliniques, en collaboration avec les professionnels de santé et les laboratoires de séquençage, SeqOIA et AURAGEN. Leur action permet d’assurer une transition fluide vers une médecine plus personnalisée, tout en garantissant la qualité et la sécurité des parcours de soins.
 Avec plus de 58 000 prescriptions traitées depuis le début du plan, les CPG ont démontré leur valeur ajoutée dans l’implémentation de la médecine génomique. Leur rôle, unique en Europe, pourrait inspirer d’autres pays confrontés aux mêmes enjeux de coordination et d’équité territoriale. En France, la poursuite de ce dispositif constitue un des enjeux majeurs pour la suite du PFMG.
Avec plus de 58 000 prescriptions traitées depuis le début du plan, les CPG ont démontré leur valeur ajoutée dans l’implémentation de la médecine génomique. Leur rôle, unique en Europe, pourrait inspirer d’autres pays confrontés aux mêmes enjeux de coordination et d’équité territoriale. En France, la poursuite de ce dispositif constitue un des enjeux majeurs pour la suite du PFMG.
 Mme M, patiente de 71 ans, est prise en charge en 2020 pour un carcinome canalaire infiltrant de grade II du sein droit, surexprimant les récepteurs aux oestrogènes (RO+) sans surexpression des récepteurs à la progestérone (RP-), ERBB2 (HER2) non amplifié, traitée par mastectomie puis hormonothérapie par Létrozole. Par ailleurs, elle présentait depuis 2016, un nodule parenchymateux pulmonaire lobaire supérieur gauche d’évolution très lente, non biopsiable, non opérable, qui a été finalement irradié, également en 2020.
En 2022 apparait un nodule sous-cutané para-ombilical gauche pour lequel est effectuée une exérèse. L’examen anatomopathologique retrouve un adénocarcinome infiltrant dont les aspects histologiques et immunohistochimiques ne s’accordent pas avec une origine mammaire, ni clairement avec un autre primitif. Il s’agit donc ici d’un adénocarcinome de primitif inconnu (CUP).
Les explorations secondaires mettent en évidence de multiples lésions dont cérébrales, ganglions cervicaux, pulmonaires et de la sphère ORL. Plusieurs hypothèses cliniques sont retenues dont le carcinome des glandes salivaires ou un adénocarcinome pulmonaire.
Devant ce tableau, le cas est présenté plusieurs fois en RCP nationale CUP avec proposition d’analyse moléculaire dans le cadre du Plan France Médecine Génomique. Une première analyse est effectuée sur le nodule sous-cutané para-ombilical en FFPE, et une nouvelle biopsie d’un nodule cervical gauche accessible est programmée pour disposer d’une analyse plus approfondie sur matériel congelé.
Dans les 2 cas, l’analyse moléculaire retrouve un variant pathogène dans les gènes SETD2, PIK3CA, ARID2, et DNMT2B, ainsi qu’un variant pathogène associé à une perte du deuxième allèle dans le gène STAG2. L’analyse du profil d’expression des gènes, sur tissu congelé par l’outil TransCUPtomics (
Mme M, patiente de 71 ans, est prise en charge en 2020 pour un carcinome canalaire infiltrant de grade II du sein droit, surexprimant les récepteurs aux oestrogènes (RO+) sans surexpression des récepteurs à la progestérone (RP-), ERBB2 (HER2) non amplifié, traitée par mastectomie puis hormonothérapie par Létrozole. Par ailleurs, elle présentait depuis 2016, un nodule parenchymateux pulmonaire lobaire supérieur gauche d’évolution très lente, non biopsiable, non opérable, qui a été finalement irradié, également en 2020.
En 2022 apparait un nodule sous-cutané para-ombilical gauche pour lequel est effectuée une exérèse. L’examen anatomopathologique retrouve un adénocarcinome infiltrant dont les aspects histologiques et immunohistochimiques ne s’accordent pas avec une origine mammaire, ni clairement avec un autre primitif. Il s’agit donc ici d’un adénocarcinome de primitif inconnu (CUP).
Les explorations secondaires mettent en évidence de multiples lésions dont cérébrales, ganglions cervicaux, pulmonaires et de la sphère ORL. Plusieurs hypothèses cliniques sont retenues dont le carcinome des glandes salivaires ou un adénocarcinome pulmonaire.
Devant ce tableau, le cas est présenté plusieurs fois en RCP nationale CUP avec proposition d’analyse moléculaire dans le cadre du Plan France Médecine Génomique. Une première analyse est effectuée sur le nodule sous-cutané para-ombilical en FFPE, et une nouvelle biopsie d’un nodule cervical gauche accessible est programmée pour disposer d’une analyse plus approfondie sur matériel congelé.
Dans les 2 cas, l’analyse moléculaire retrouve un variant pathogène dans les gènes SETD2, PIK3CA, ARID2, et DNMT2B, ainsi qu’un variant pathogène associé à une perte du deuxième allèle dans le gène STAG2. L’analyse du profil d’expression des gènes, sur tissu congelé par l’outil TransCUPtomics (