Mme M, patiente de 71 ans, est prise en charge en 2020 pour un carcinome canalaire infiltrant de grade II du sein droit, surexprimant les récepteurs aux oestrogènes (RO+) sans surexpression des récepteurs à la progestérone (RP-), ERBB2 (HER2) non amplifié, traitée par mastectomie puis hormonothérapie par Létrozole. Par ailleurs, elle présentait depuis 2016, un nodule parenchymateux pulmonaire lobaire supérieur gauche d’évolution très lente, non biopsiable, non opérable, qui a été finalement irradié, également en 2020.
En 2022 apparait un nodule sous-cutané para-ombilical gauche pour lequel est effectuée une exérèse. L’examen anatomopathologique retrouve un adénocarcinome infiltrant dont les aspects histologiques et immunohistochimiques ne s’accordent pas avec une origine mammaire, ni clairement avec un autre primitif. Il s’agit donc ici d’un adénocarcinome de primitif inconnu (CUP).
Les explorations secondaires mettent en évidence de multiples lésions dont cérébrales, ganglions cervicaux, pulmonaires et de la sphère ORL. Plusieurs hypothèses cliniques sont retenues dont le carcinome des glandes salivaires ou un adénocarcinome pulmonaire.
Devant ce tableau, le cas est présenté plusieurs fois en RCP nationale CUP avec proposition d’analyse moléculaire dans le cadre du Plan France Médecine Génomique. Une première analyse est effectuée sur le nodule sous-cutané para-ombilical en FFPE, et une nouvelle biopsie d’un nodule cervical gauche accessible est programmée pour disposer d’une analyse plus approfondie sur matériel congelé.
Dans les 2 cas, l’analyse moléculaire retrouve un variant pathogène dans les gènes SETD2, PIK3CA, ARID2, et DNMT2B, ainsi qu’un variant pathogène associé à une perte du deuxième allèle dans le gène STAG2. L’analyse du profil d’expression des gènes, sur tissu congelé par l’outil TransCUPtomics (Vibert et al., 2021) montre que le profil transcriptomique de cette tumeur est compatible avec celui d’un adénocarcinome bronchique (Figure 1).
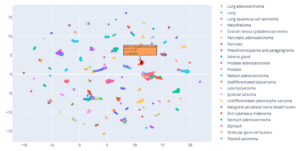
Figure 1: Résultat TransCUPtomics
Au cours de la RCP nationale CUP d’aval, l’ensemble des données moléculaires, cliniques et immunohistochimiques sont confrontées et les expertises réunies à cette RCP tranchent pour une origine pulmonaire de cette tumeur. Ce résultat conforte le traitement envisagé par Carboplatine, Taxol et Pembrolizumab, adapté à un contexte de cancer du poumon.
Sous ce traitement, la patiente a présenté une réponse partielle significative, avec une régression nette des adénopathies médiastinales et une quasi-disparition du nodule pré-scapulaire gauche, associées à une stabilité des nodules pulmonaires.
Toutefois, une nouvelle évaluation à 6 mois a mis en évidence une progression tumorale cérébrale et extra-encéphalique ganglionnaire, justifiant la mise en place d’une radiothérapie cérébrale avec une reprise du pembrolizumab en monothérapie.
L’analyse moléculaire, en identifiant la mutation activatrice du gène PIK3CA pourra permettre l’accès à des essais cliniques pan-tumeurs en cas d’évolution.
Ce cas clinique illustre l’apport du séquençage simultané de l’ADN et de l’ARN tumoral dans le cadre du PFMG2025 afin d’obtenir une caractérisation exhaustive de la tumeur permettant une aide au diagnostic et au choix de la stratégie thérapeutique pour les cancers de primitif inconnu.

